반응형
▶ FDA에서 의료기기 사이버보안과 관련된 가이드라인을 발표함
▶ 적용해야 되는 인허가 프로세스: 510(k), De Novo, PMA, PDP, IDE, HDE, BLA, IND
▶ 적용제품: Software, Hardware and firmware
▶ 생산 전, 생산 후 단계를 고려하여 품질경영시스템 (QSR)에도 반영 되어야 함
▶ 인허가를 위해 필요한 서류와 점검 단계를 설명
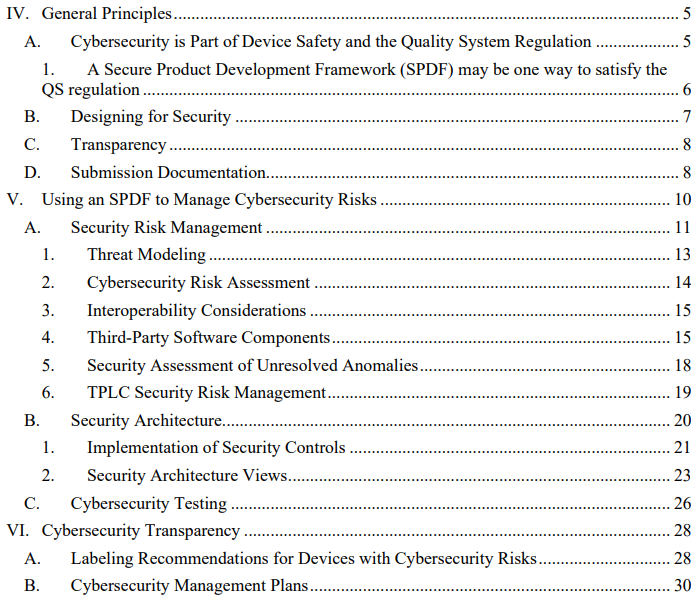
Cybersecurity: Quality System Considerations and Premarket Submissions
This document provides FDA’s recommendations regarding premarket submissions of devices with cybersecurity risk.
www.fda.gov

반응형
'미국 FDA' 카테고리의 다른 글
| [FDA] Electronic submission template for medical device 510(k) submissions (1) | 2023.10.05 |
|---|---|
| [FDA] Cybersecurity in medical devcies Frequently asked Questions (FAQs) (0) | 2023.10.04 |
| [FDA] CDRH - International Harmonization Strategic Plan (0) | 2023.09.25 |
| [FDA] Digital Health Frequently Asked Questions (0) | 2023.09.18 |
| [FDA] ISO 10993-1 가이던스 발행 (0) | 2023.09.12 |