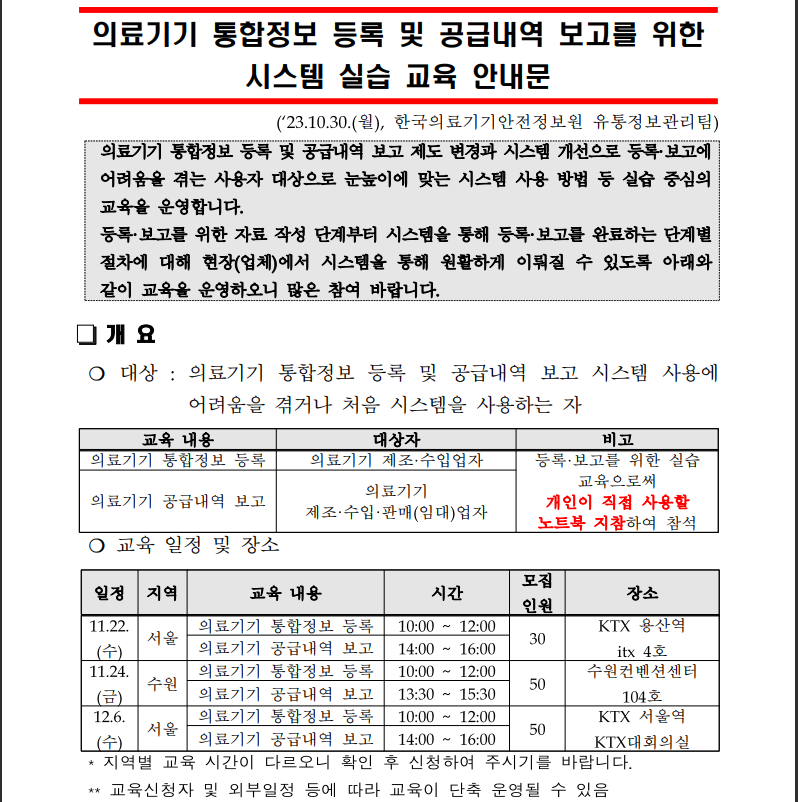
▶ 식품의약품안전처에서 아래와 같이 혁신의료기기 지정결과를 공고함 ▶ 혁신의료기기 지정 공고 내용 1. (주)솔메딕스 (일반 제52호): 첨단기술군 - 품목군: 멸균주사침 - 제품명/모델명: Lightin / LI-23G-50 외 5건 식품의약품안전처>알림>공지/공고>공고 - 상세보기 | 식품의약품안전처 (mfds.go.kr) 식품의약품안전처>알림>공지/공고>공고 | 식품의약품안전처 혁신의료기기 지정 공고(일반 제52호) 등록일 2023-11-23 조회수 99 식품의약품안전처 공고 제 2023-548호 「의료기기산업 육성 및 혁신의료기기 지원법」제21조 및 같은 법 시행령 제15조에 따라 혁신 www.mfds.go.kr